Древние цивилизации уже задолго до своего «официального» открытия начали использовать антибиотики интуитивно. Они лечились травами, медом, животными продуктами, и не редко испорченные «лекарства» оказывались наиболее эффективными: плесневелый хлеб, скисшее молоко, стухшее мясо.
В древности люди интуитивно использовали естественные средства, содержащие антибиотики.
Их положительное действие состояло в том, что они содержали плесень, которая обладала антимикробными свойствами и защищала организм от вредных воздействий окружающей среды.
Греки использовали плесневелый хлеб для дезинфекции ран и лечения кожных воспалений, а в Древней Руси в качестве антисептика применяли теплую землю.
В Междуречье медики подавали больным закисший суп с черепашьими панцирями и змеиными шкурами, а глазные заболевания лечили компрессами, составленными из смеси лягушачьей желчи и кислого молока.
Только через столетия врачи и ученые осознали, что причина гнойных ран и многих заболеваний – невидимые глазу существа (бактерии), которые могут проникнуть в организм через грязные руки или медицинские инструменты.
Открытие бактерий случилось благодаря голландскому ученому Антони ван Левенгуку, который изготовил первый микроскоп.

Первый в мире микроскоп, созданный Антони ван Левенгуком
Для поиска средств борьбы с бактериями исследователи снова прибегли к древнему “лекарству” и начали тщательно изучать целебные свойства плесени.
В XVII–XIX веках англичане проводили активные исследования с различными видами плесени и установили, что бактерии не растут на посевах, покрытых этим грибком. В 1897 году во Франции Эрнест Дюшен вылечил морских свинок от брюшного тифа с использованием плесени (Penicillium glaucum). Он разбавлял ее водой и вводил лабораторным животным.

Лечебная плесень Penicillum glaucum, с которой экспериментировал Эрнест Дюшен, до сих пор применяется для производства сыра горгондзола
В различных уголках земного шара исследователи обнаруживали полезный гриб плесени и экспериментировали с лечением распространенных инфекций. При этом достигали неплохих результатов. Однако эпохальное открытие антибактериальных свойств грибов-плесневиков было признано гораздо позднее.
Великая нечистоплотность Флеминга
В 1928 году сэр Александр Флеминг проводил исследования в своей лаборатории в Англии с бактериями семейства Staphylococcaceae (стафилококки). Ученый выращивал большое количество колоний в чашках Петри, а затем решил сделать перерыв — отправился в отпуск. При этом посуду с экспериментами он не вымыл как следует, а некоторые чашки даже лежали несколько недель нетронутыми.
По возвращении ученого, он заметил, что посевы покрылись плесенью, но вокруг плесневых “шапок” совсем не было бактерий.
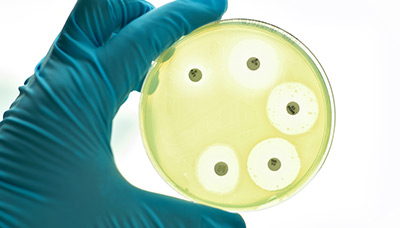
Плесень в чашке с колонией бактерий. Прозрачные круги — области, где действует пенициллин
Флеминг исследовал опасную плесень и понял, что бактерии погибли из-за её специфического «сока», который она выделяет. Ученый назвал его пенициллином, в честь Penicillus, плесени, уничтожившей стафилококки.
Александр Флеминг не смог получить чистый пенициллин (в экспериментах использовался отфильтрованный «бульон»), не смог определить вид целебной плесени (спустя 2 года выяснилось, что это Penicillium notatum), однако в подробностях описал, как она воздействует на разные бактерии, сравнил разные виды плесени, и, что самое главное, сохранил образцы и отправил их заинтересованным ученым.
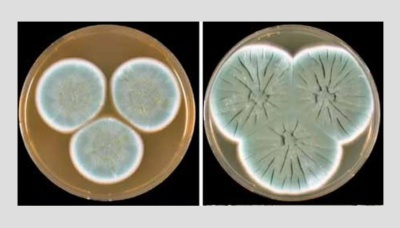
Изучение колоний плесени рода Penicillus, с которыми работал Флеминг. Фото: Houbraken, J., Frisvad, J.C. & Samson, R.A
Один такой образец пролежал почти 10 лет в Оксфордском университете. В 1939 году ученый Эрнст Чейн извлек из него чистый пенициллин, а его наставник Говард Флори успешно протестировал препарат на животных.
Поднос, благодаря которому Флеминг сделал открытие, вместе с той самой плесенью в 2017 году продали на аукционе за 14 тысяч долларов.
Первым испытуемым стал 45-летний офицер полиции из Англии по имени Альберт Александр. Это случилось в декабре 1940 года, когда он поранился шипом розы в своем саду и заразился стафилококковой и стрептококковой инфекцией. На момент начала эксперимента в феврале 1941 года его состояние было крайне тяжелым, ни один из используемых методов лечения не помогал: инфекция продолжала распространяться по его телу, лицо было покрыто гнойными язвами, а один глаз пришлось удалить.

Александр Флеминг в своей лаборатории
Уже после первых суток после начала применения пенициллина состояние Альберта резко улучшилось: уменьшилось гноение, опустилась температура. Однако запасов лекарства у ученых не хватало для завершения полного курса лечения.
Исследователи производили отфильтрованную мочу пациента, чтобы получить даже малейшие следы пенициллина. Этого оказалось недостаточно, и Альберт Александр умер от сепсиса.
Несмотря на потенциальные возможности использования пенициллина, британские фармацевтические компании не проявили особого интереса к производству нового лекарства из-за огромного количества оборонных заказов. Чтобы не утратить открытие, ученые решили передать его Соединённым Штатам, однако это было очень рискованно, поскольку такое перспективное лекарство могло изменить исход войны, и поэтому нельзя было позволить его попасть в руки фашистов.
Для того чтобы вывезти образцы плесени, британцы придумали хитроумный план: они пропитали пальто грибными спорами и таким образом доставили открытие за океан.
Колонии плесневых грибов рода Penicillium в чашках Петри
В Соединенных Штатах проявили большой интерес к пенициллину и даже нашли его американского родственника – плесень, выделяющую в 6 раз больше лечебного вещества. Плесень начали выращивать в огромных емкостях и отправлять на фронт. К концу 1942 года американские лаборатории синтезировали менее 100 доз пенициллина, в 1943-м уже выпустили 21 миллиард доз, а в 1945-м – 6,8 триллиона доз.

Эрнст Чейн (слева) и Говард Флори (справа). Лауреаты Нобелевской премии по физиологии и медицине 1945 года (совместно с А. Флемингом)
После того, как пенициллин показал свой успех, ученые по всему миру начали активно искать другие антибиотики. Так, в 1952 году на острове Борнео были обнаружены микроорганизмы Streptomyces orientalis, из которых был выделен ванкомицин. Применение этого препарата началось в 1958 году. К тому времени уже в 1960-х годах появились цефалоспорины – улучшенные формы пенициллинов, борющиеся с устойчивыми к антибиотикам бактериями.
Благодаря открытию антибиотиков средняя продолжительность жизни в период с 1944 по 1972 год увеличилась на 8 лет. Это в основном произошло благодаря тому, что дети и молодые люди перестали умирать от ранее неизлечимых инфекций.
Механизм действия антибиотиков на бактерии
Действие антибиотиков на бактерии происходит двумя способами: либо они разрушают клеточную стенку, либо воздействуют на генетический аппарат микроорганизмов.
Антибиотики, разрушающие клеточную стенку
Окруженная клеточной стенкой, микроорганизм защищен от вредных факторов окружающей среды, поддерживает свою форму и контролирует внутренний баланс жидкости и питательных веществ. Если бы не клеточная стенка, бактерии погибли бы от изменений pH, нарушения водного баланса, воздействия температуры и других агрессивных факторов.
Среди них – β-лактамы (пенициллины, цефалоспорины, карбопенемы), гликопептиды (ванкомицин), полимиксины (колистин). Эти антибиотики применяются для лечения широкого спектра инфекций, включая гонорею, хламидиоз, некоторые кишечные инфекции, пневмонию.
Колистин известен как один из наиболее мощных антибиотиков, препарат “последней надежды”. Его применяют при лечении инфекций, вызванных устойчивыми госпитальными микроорганизмами, а также в случаях, когда другие антибактериальные препараты оказываются бессильными.
Этимология слова «антибиотик» происходит от греческих корней ἀнτί («против») и βίος («жизнь»).
Препараты, уничтожающие генетический аппарат бактерий
Некоторые лекарства против бактерий могут проникать в «сердце» микроорганизмов и нарушать процессы синтеза ДНК, передачи генетической информации, образования белков, необходимых для построения клетки бактерий. Как следствие, бактерии теряют возможность размножаться и расти.
В этот класс входят тетрациклины, макролиды, фторхинолоны, сульфаниламиды. Их использование распространено при туберкулезе, туляремии, чуме, бруцеллезе, сепсисе, раневых и ожоговых инфекциях, а также других бактериальных заболеваниях.
Однако спектр действия антибиотиков может быть узким или широким. Препараты с узким спектром действия борются только с определенными бактериями, например, с одним только видом стафилококка. Их прописывают в тех ситуациях, когда известно, какая бактерия вызвала инфекцию.
Антибиотики широкого спектра действия сражаются сразу с несколькими видами бактерий, поэтому их обычно используют, когда нет времени на поиски «виновника» инфекции и необходимо начать лечение как можно быстрее.
При этом антибиотики уничтожают не только патогенные бактерии, но и представителей нормальной микрофлоры кишечника.
Сценарий без выхода: когда без антибиотиков не обойтись
Использование антибиотиков – это не просто метод лечения инфекционных заболеваний. Применение антибактериальной терапии распространено в различных областях медицины, включая хирургию, неонатологию, онкологию и другие.
Устранение инфекционных заболеваний
Благодаря антибиотикам люди перестали умирать от раневых инфекций
Появление антибиотиков стало настоящим прорывом в медицине: многие заболевания, вызванные патогенными бактериями, больше не являются смертельными, а стали излечимыми. Это позволило снизить смертность от раневых, нейроинфекций, пневмонии, а также инфекций, передающихся половым путем.
Каждый день в мире более миллиона людей в возрасте от 15 до 49 лет заражаются ИППП. Применение антибиотиков предотвращает летальные исходы от таких инфекций и их последствий.
Хирургия
Использование антибиотиков перед операцией – это эффективный способ предотвратить осложнения и ускорить процесс восстановления
Все операции, даже самые маленькие, например удаление фурункула, без использования антибиотиков становятся очень опасными. Потому что любая открытая рана – это идеальный путь для инфекции, поскольку бактерии или другие патогены могут проникнуть прямо в кровь, обходя защитные механизмы организма.
Акушерство и неонатология

Развитие инфекций может привести к трагическим последствиям для плода, задержке его здорового роста и нарушениям в развитии. Применение антибиотиков способно спасти и матери, и ребенка.
Особенно подвержены риску заражения инфекциями в родильном зале или отделении реанимации дети со слабым иммунитетом, недоношенные и новорожденные от инфицированных матерей. Однако и здоровым, своевременно родившимся младенцам угрожают серьезные инфекции.
Их иммунная система находится на стадии формирования и еще неспособна полноценно защищать организм от патогенных микроорганизмов и других угроз. Поэтому до изобретения антибиотиков детская смертность оставалась довольно высокой.
Дополнительно, около 15–20% всех родов в мире проходят с применением кесарева сечения. Необходимо сделать разрез брюшной стенки, чтобы безопасно вынуть младенца. Этот разрез может представлять потенциальную опасность, так как инфекции могут попасть в открытую рану.
Женщинам с осложнениями беременности и угрозой прорыва плодовых оболочек проводится профилактическое антибиотикотерапия, чтобы избежать серьезных инфекционных осложнений у матери и ребенка. Без антибиотиков такая профилактика будет невозможна.
Лечение онкологических заболеваний

Применение антибиотиков помогает ослабленной иммунной системе онкопациентов бороться с возможными инфекциями и их последствиями
Известными методами борьбы с раком являются химиотерапия и радиотерапия. Однако оба эти метода наносят серьезный ущерб иммунной системе пациента. Поэтому организм становится более уязвимым перед даже незначительными инфекциями, а взаимодействие с бактериальной флорой может быть фатальным.
Для пациентов, проходящих лечение от онкологии, может быть предложено использование антибиотиков в профилактических целях, чтобы избежать возможных опасных последствий.
Трансплантология
Для предотвращения отторжения пересаженных органов и тканей пациенты вынуждены принимать препараты, подавляющие иммунную систему. Это приводит к тем же проблемам, что и при лечении рака: организм неспособен бороться с патогенными бактериями, вирусами и грибами. Без использования антибиотиков риск развития инфекций повышается во время периода принятия трансплантата.
Почему антибиотики перестают работать
В 1980-х годах не появилось ни одного нового класса антибиотиков, ученые лишь вносят изменения в уже существующие препараты. Это обусловлено несколькими причинами. Среди главных – наличие достаточного разнообразия существующих лекарств и экономическая невыгодность производства антибактериальных средств.
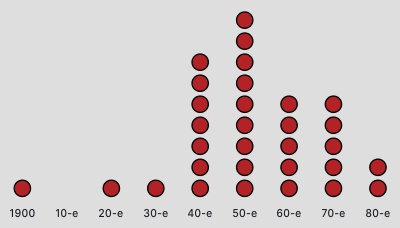
Количество разработанных антибиотиков в разные периоды ХХ века. Последний был открыт в 1984 году (по данным информагентства Bloomberg)
За последние два десятилетия многие известные фармацевтические компании, такие как Johnson & Johnson, Roche, Pfizer, Eli Lilly and Company, Bristol-Myers Squibb, сократили разработку новых антибиотиков или прекратили проекты в этой области. Причина заключается в появлении других перспективных и в то же время более прибыльных направлений. Например, производство лекарств для лечения хронических заболеваний, таких как сахарный диабет, артериальная гипертензия, депрессия.
По средним показателям, антибиотики начинают окупаться только через двадцать три года после выпуска. Кроме того, для запуска одного препарата компании требуется около одного миллиарда долларов.
Исследование нового препарата — это очень дорогое мероприятие, так как, помимо необходимости провести тесты в лаборатории, необходимо проверить его эффективность и безопасность на людях, пройти многочисленные проверки со стороны регулирующих органов. В результате лишь незначительное количество из изученных молекул попадает на рынок. После таких испытаний производящая компания, естественно, стремится получить прибыль.
Однако, учитывая, что бактерии очень быстро развивают устойчивость к новым лекарствам, имеется высокий риск того, что перспективный препарат в ближайшее время станет неэффективным и просто перестанет действовать. В случае с препаратами для лечения хронических неинфекционных заболеваний, риски на порядок ниже.
Мутация бактерий
Для выживания бактерии развивают способность мутировать и приобретать новые навыки, которые помогают им противостоять враждебным условиям окружающей среды. Некоторые научились обходиться без кислорода, другие вырастили жгутики для передвижения, третьи развили толстую “броню”, а четвертые научились производить ферменты, разрушающие антибиотики. Учитывая, что бактерии – организмы с коротким жизненным циклом, которые выживают за счет своего быстрого размножения, новые способности быстро наследуются потомками.
Процесс деления бактерий в благоприятных условиях очень интенсивен: в среднем каждый час у одной клетки появляется дочерняя копия.
За сутки у бактерии может появиться столько поколений “наследников”, сколько людей родилось с времен Ивана Грозного.
Полезные для выживания мутации могут передаваться бактериями не только дочерним клеткам, но и другим организмам. Этот процесс известен как горизонтальный перенос генов. Так, бактерии, обладающие защитным механизмом, могут передать его «соседним» бактериям, даже не являющимся родственниками.
Наблюдения Флеминга также указывают на то, что некоторые бактерии научились сопротивляться пенициллину и последующим антибиотикам. Это привело к усложнению процесса разработки новых антибиотиков с течением времени.
Как антибиотикорезистентность приводит к тому, что человечество становится беззащитным перед инфекциями
В 1946 году выявили резистентность к пенициллину у 14% заболевших, к 1950-му – уже у 59%, а к 1990-му – у 95%, поэтому было необходимо разрабатывать новые формулы пенициллинов следующих поколений для поддержания эффективности лечения. Сейчас ВОЗ выделяет устойчивость к антибиотикам как одну из основных опасностей для мирового здравоохранения. По оценкам специалистов, каждый год из-за устойчивости становится все сложнее лечить различные инфекции, такие как пневмония, туберкулез, гонорея, сальмонеллез.
От устойчивости к антибиотикам умирает 700 000 человек ежегодно. Прогнозируется, что к 2050 году это число вырастет до 10 миллионов. То есть бактерии, стойкие к антибиотикам, приведут к большему количеству летальных исходов, чем рак.
Бактерии, устойчивые к антибиотикам:
- бактерия ацинетобактер (Acinetobacter baumannii),
- возбудитель заболевания синегнойная палочка (Pseudomonas aeruginosa),
- группа бактерий энтеробактерии (Enterobacteriaceae),
- бактерия энтерококк фэциум (Enterococcus faecium),
- патогенный золотистый стафилококк (Staphylococcus aureus),
- бактерия хеликобактер пилори (Helicobacter pylori),
- бактерия кампилобактер (Campylobacter),
- патогенная сальмонелла (Salmonella),
- бактерия гонококк (Neisseria gonorrhoeae),
- возбудитель пневмонии пневмококк (Streptococcus pneumonia),
- бактерия гемофильная палочка (Haemophilus influenzae),
- бактерия шигелла (Shigella),
- бактерия клебсиелла пневмонии (Klebsiella pneumonia),
- бактерия кишечная палочка (Escherichia coli),
- метициллинустойчивые штаммы золотистого стафилококка (MRSA).
Ежегодно от устойчивого к антибиотикам туберкулёза погибает около 250 тысяч человек.
Распространение устойчивости
MRSA
Более 50 лет назад появились штаммы золотистого стафилококка, устойчивые к антибиотику метициллину, известные как MRSA (Methicillin-resistant Staphylococcus aureus). Эти бактерии чаще других становятся нечувствительными к антибиотикам и уносят жизни более 15 тысяч человек каждый год.
Энтерококки, устойчивые к ванкомицину, – причина госпитальных инфекций. В США ежегодно регистрируется около 66 тысяч случаев заражения этими энтерококками.
Стрептококк пневмонии Streptococcus pneumoniae, который устойчив к амоксициллину и азитромицину, может вызвать серьезное воспаление легких и менингит. Сопротивляемость усложняет лечение и приводит к семитысячам смертей ежегодно.
Появление устойчивости бактерий — естественный процесс, но специалисты отмечают, что человечество зачастую ускоряет этот процесс.
Неконтролируемое применение антибиотиков
На протяжении многих лет антибиотики были легкодоступными, поэтому люди применяли их для любых недомоганий: от простуды до поноса. Это привело к появлению новых устойчивых бактерий, которые оказались нечувствительными к имеющимся антибактериальным препаратам.
Антибиотики эффективны только в борьбе с бактериями, поэтому они не помогут при вирусных инфекциях (за исключением бактериальной суперинфекции). Однако многие люди продолжают принимать антибиотики без необходимости.
Нарушение рекомендаций по приему антибиотиков также может привести к развитию устойчивости возбудителя. Часто пациенты не принимают антибиотики достаточно долго или в нужной дозе, они прекращают прием препарата после снижения симптомов, не завершая полный курс лечения по собственной инициативе. При этом бактерии не полностью удаляются из организма, но они знакомятся с антибиотиком и развивают механизмы устойчивости.
Недостаточная концентрация антибиотика не позволяет убить бактерии, но помогает им приспособиться к препарату, как к неблагоприятному фактору, такому как холод или изменение pH.
Использование антибиотиков не всегда обосновано, не только в случае простуды, но и при других заболеваниях. Например, они часто применяются в гинекологии и урологии. Один из классических примеров – обнаружение большого количества патогенных бактерий в анализе мочи при бессимптомной бактериурии. При этом у человека нет никаких жалоб.
Антибиотики часто назначаются пациентам для лечения воспаления, но это не изменяет жизнь человека, а лишь способствует “тренировке” бактерий. Последние исследования показали, что бессимптомная бактериурия является видом комменсализма (безопасного сожительства бактерий в организме хозяина). Она может даже быть полезной для поддержания перекрёстного иммунитета к другим бактериям. Поэтому многие эксперты считают, что это состояние не требует лечения, если не проявляет симптомов (принцип “не лечить анализы”). Пациентов с бессимптомной бактериурией стоит наблюдать в динамике.
В развитых странах где после 2020 года около 216 миллионов избыточных доз антибиотиков было продано, эти препараты редко доступны без рецепта врача. Тем не менее, бактерии все равно развивают устойчивость к ним. Это во многом связано с тем, что в некоторых странах, включая Индию, такую медицинскую продукцию все еще можно приобрести свободно.
Индия занимает лидирующие позиции по среди всех стран по заболеваниям, вызванных устойчивыми к антибиотикам штаммами бактерий. Более половины образцов клебсиеллы пневмонии в этой стране оказались устойчивыми к карбапенемам, антибиотикам широкого спектра действия.
Общее потребление антибиотиков с 2000 по 2010 год увеличилось более чем в три раза. Основную часть этого увеличения вызвали пять стран – Бразилия, Россия, Индия, Китай и Южно-Африканская Республика (БРИКС).
Одно предупреждение должно быть услышано. Пенициллин, несмотря на все свои полезные свойства, не является абсолютно безвредным, поэтому не стоит расслабляться и не бояться возможного передозирования. Опасность заключается в малых дозах этого препарата. Вполне возможно вырастить устойчивые к пенициллину микроорганизмы в лабораторных условиях, просто выживая при концентрациях, которые не могут их уничтожить, и это же самое может случайно произойти в организме.
В ближайшее время пенициллин станет доступным каждому, и есть опасность, что некомпетентный человек может легко принять недостаточное количество препарата и вырастить в организме микроорганизмы, стойкие к антибиотику, из-за постоянного воздействия низких концентраций лекарства.
Аграрный сектор
Известно, что применение антибиотиков необходимо не только для лечения людей, но и для поддержания производства. Так, использование антибиотиков в животноводстве помогает эффективно лечить животных, поддерживать благоприятное эпидемиологическое состояние и обеспечивать безопасность продуктов животноводства. Интересно, что для этих целей применяются те же группы антибиотиков, которые применяются для лечения инфекций у людей.

По крайней мере, половина всех производимых антибиотиков используется в сельском хозяйстве
В результате бактерии, которые стали устойчивыми в организме животных, могут передаваться и на человека: через непосредственный контакт, окружающую среду или продукты (молоко, яйца, мясо).
Часто специалисты из Роспотребнадзора обнаруживают антибиотики при проверке молочной и мясной продукции, таких как сметана, кефир, полуфабрикаты из курицы и свинины.
Фактически, применение антибиотиков для лечения животных не так опасно, главное – соблюдать правила безопасности. После лечения и пары недель отдыха животное должно быть «отдохнуть»: мясо и другие продукты, полученные от него, не должны попасть в производство. За этот период антибиотики выводятся из организма. Однако это временное затруднение, которое приводит к потере прибыли. Некоторые фермеры игнорируют эти меры предосторожности, что приводит к появлению антибиотиками насыщенной продукции на прилавках.
Помимо традиционных продуктов животного происхождения, антибиотики также обнаруживаются в мясе рыбы и некоторых морепродуктах. Оказалось, что вода в каналах Санкт-Петербурга обладает выраженным антимикробным действием. Причина в том, что антибиотики поступают в нее из очистных сооружений.
В результате, например, гладкие поверхности водоемов лишились защитного слоя слизи. В новых условиях она оказалась просто ненужной, ведь они плавают в растворе антибиотиков.
Следы антибиотиков были обнаружены даже в меде. Специалисты высказали предположение, что пчеловоды могут применять препараты для профилактики и лечения аскосфероза – инфекционного заболевания, которое поражает личинок трутней и молодых пчел.
Бактерии-монстры
Микробы, обладающие устойчивостью к любым известным антимикробным препаратам, получили название супербактерий. Это открытие было сделано недавно.
В 2008 году в индо-пакистанском регионе человечество столкнулось с бактериальной инфекцией, нечувствительной к антибиотикам. Хоть случаи были единичными, но сам факт полирезистентности насторожил медиков и ученых.
В 2010 году стало известно, что супербактерии распространены по всему миру. Предполагается, что люди приносят опасные штаммы из индо-пакистанского региона при возвращении из поездок.
В 2016 году 70-летняя женщина из Америки вернулась из путешествия в Индию. Во время поездки она сломала ногу, попала в местную больницу и там заразилась супербактерией Klebsiella pneumoniae. Боль в ноге не утихала, а по возвращении из путешествия у женщины началось сильное воспаление. В американской больнице врачи применили все известные на тот момент антибиотики, однако ни один из 26 препаратов не помог. В итоге женщина скончалась от септического шока.
Позже случаи заражения также были выявлены в Швеции, Бельгии, США, Канаде, Великобритании. Специалисты утверждают, что большинство зараженных заразились именно во время пребывания в медицинских учреждениях.
В больницах используется широкий спектр антибактериальных препаратов, а также антисептиков, поэтому бактерии развивают устойчивость к многим из них и быстро передаются между пациентами и персоналом.
Пути преодоления антибиотикорезистентности
В каждой стране существуют собственные методы решения данной проблемы. Например, в Европейском Союзе с 2006 года запрещено добавление антибиотиков в корма для животных. В России с 2017 года ограничено применение антибактериальных средств: их продажа без рецепта врача запрещена в аптеках. В феврале 2018 года Всемирная организация здравоохранения выпустила рекомендации о том, как противостоять антибиотикорезистентности, для различных участников лечебного процесса: пациентов, врачей, фармацевтов, представителей власти, фармацевтических компаний и сельского хозяйства.
Основные правила преодоления антибиотикорезистентности для пациентов:
- следуйте указаниям врача и принимайте антибиотики полностью;
- не передавайте антибиотики другим людям;
- соблюдайте гигиену при приготовлении пищи и мойте руки;
- избегайте контакта с больными;
- практикуйте безопасный секс;
- вакцинируйтесь полностью.
Для медиков существуют рекомендации по рациональному применению антибиотиков – актуальные справочники, где указано, каким образом и в каких случаях следует использовать антибиотики. Например, при инфекции Х начинайте с препарата А, при неэффективности – переходите к препарату Б, и только потом к препарату В. Препараты второй и последующих линий применяются только по необходимости.
В начале лечения обычно прописывается антибиотик широкого спектра, а затем (после получения результатов посева на чувствительность к антибиотикам) его можно заменить на препарат суженного спектра. При недостаточной эффективности применяются комбинации антибиотиков.
Препараты первой линии, как правило, легче переносятся, стоят дешевле и имеют обширное научное обоснование. При нерациональном использовании антибиотиков возрастает риск перехода на препараты следующих линий и последний шанс, после которого уже нечего применить.
Подбирать антибиотик, который с вероятностью 99% поможет победить бактерию, можно только по результатам посева с определением чувствительности к антибиотикам.
Альтернатива антибиотикам
Существуют и другие способы защиты от инфекционных заболеваний, не связанные с антибиотиками.
Методы предотвращения и лечения инфекционных заболеваний:
- пассивная иммунизация (введение препаратов с готовыми антителами);
- активная иммунизация (вакцинация);
- фаговая терапия (лечение с помощью вирусов, например бактериофагов);
- применение антисептиков.
Бактериофаги — это вирусы, которые уничтожают бактерии, но не повреждают другие живые существа
Один из самых многообещающих методов борьбы с бактериями — это фаговая терапия. Каждый вид бактериофагов (а их миллионы) действует исключительно против определенного вида бактерий. В отличие от процесса развития антибиотикорезистентности, бактериофаги способны меняться, поскольку они являются вирусами. Когда бактерия становится устойчивой к одному фагу, другой фаг может найти новый способ проникнуть в нее и победить.
Как и антибиотики, бактериофаги являются антибактериальными средствами. В общем, и те, и другие уничтожают бактерии, но делают это по-разному. Бактериофаги не могут полностью заменить антибиотики, поскольку каждый из них действует только против определенного вида бактерий. Однако в большинстве случаев пациенту все равно требуется антибактериальная терапия на этапе, когда возбудитель еще не определен.
Недостаточно крупных исследований, подтверждающих эффективность и безопасность фаговой монотерапии, пока не хватает.
Для повышения эффективности антимикробной терапии и предотвращения антибиотикорезистентности бактериофаги начали использовать в сочетании с антибиотиками. Оказалось, что их общее действие превышает сумму эффектов каждого препарата по отдельности.
Возможно ли остановить распространение антибиотикорезистентности
До тех пор, пока антибиотики не перестанут действовать, они остаются самым эффективным способом лечения бактериальных инфекций и спасают миллионы жизней ежедневно. Однако каждый раз, когда люди принимают их без необходимости и не соблюдают меры предосторожности, они способствуют развитию и распространению антибиотикорезистентности. Это влечет за собой негативные последствия: пациенты проводят больше времени в больнице, государство тратит больше денег на медицинские расходы, а люди умирают чаще всего от бактериальных инфекций и их последствий.
Поэтому, чтобы сохранить эффективность антибиотиков и избежать возвращения к Средневековью с его смертельными эпидемиями, каждому следует бережно относиться к антибактериальной терапии: принимать антибиотики только по назначению врача, строго соблюдать предписанный курс лечения и не употреблять их на всякий случай. Не соблюдая эти правила, человек помогает распространению антибиотикорезистентности, что ухудшает течение инфекции и увеличивает риск возникновения потенциально опасных побочных эффектов в десятки раз.
Роль общества в предотвращении антибиотикорезистентности
Существует стремительное развитие новых возможностей в области разработки антибиотиков для борьбы с антибиотикорезистентностью. Однако недостаток эффективности новых лекарств требует активного участия общества в предотвращении этой проблемы.
Прогресс в развитии новых антибиотиков в значительной степени зависит от уровня осведомленности и понимания общества о важности сохранения эффективности этих препаратов. Участие общества в различных программах по борьбе с антибиотикорезистентностью играет ключевую роль в успешном преодолении этой проблемы.
- Образование общества по вопросам правильного использования антибиотиков может значительно сократить вероятность возникновения резистентности к лекарствам.
- Активное поддержание программ по контролю за использованием антибиотиков в медицинских учреждениях и ветеринарной медицине также является важным шагом в предотвращении антибиотикорезистентности.
- Создание глобальных сообщественных инициатив по борьбе с антимикробной резистентностью может способствовать объединению усилий на международном уровне и способствовать развитию новых антибиотиков.
Только совместными усилиями общества и медицинского сообщества можно обеспечить эффективное противодействие антибиотикорезистентности и сохранить возможность успешного лечения инфекционных заболеваний в будущем.
Перспективы развития новых антибиотиков
Современная медицина сталкивается с возрастающей проблемой антибиотикорезистентности, когда бактерии становятся устойчивыми к действию антибиотиков. Для преодоления этой проблемы необходимы новые подходы к разработке и применению антибиотиков, которые будут эффективными и безопасными для пациентов.
- Исследования в области новых антибиотиков выходят на новый уровень благодаря использованию передовых технологий и методов.
- Новые препараты, созданные на основе инновационных молекул, могут быть более эффективными и способными преодолевать антибиотикорезистентность.
- Стремительное развитие науки и медицины позволяет ускорить процесс создания и тестирования новых антибиотиков, что является важным шагом в борьбе с инфекционными заболеваниями.
Глобальные программы по борьбе с антибиотикорезистентностью поддерживают и финансируют исследования новых антибиотиков, стимулируют сотрудничество между учеными и фармацевтическими компаниями. Такой подход способствует развитию инновационных методов лечения инфекций и предотвращению распространения антибиотикорезистентных микроорганизмов.
Глобальные программы по борьбе с антибиотикорезистентностью
Проблема антибиотикорезистентности становится все более актуальной в современном обществе. Чтобы справиться с этим глобальным вызовом, мировое сообщество разрабатывает различные программы и инициативы.
Основная цель таких программ – предотвращение распространения антибиотикорезистентности и разработка эффективных стратегий лечения инфекций. Подходы в рамках глобальных программ могут варьироваться в зависимости от региона и уровня развития здравоохранения.
Международные организации и правительства активно сотрудничают для создания согласованных действий по борьбе с антибиотикорезистентностью. Эти программы имеют стратегическое значение для сохранения эффективности антибиотиков и обеспечения здоровья населения.
Влияние антибиотиков на микробиому человека
- Прием антибиотиков может существенно изменить состав и баланс микроорганизмов, населяющих кишечник, кожу и другие органы человека. Это может привести к дисбалансу микробиома, что может в свою очередь вызвать различные заболевания и проблемы со здоровьем.
- Исследования показывают, что использование антибиотиков может привести к уменьшению разнообразия микроорганизмов в микробиоме, что может отрицательно сказаться на иммунной системе и общем здоровье человека.
- Кроме того, антибиотики могут оказать влияние на микробиому даже после завершения курса лечения, поскольку некоторые микроорганизмы могут не восстанавливаться или восстанавливаться медленно, что может способствовать развитию новых проблем со здоровьем.
Поэтому важно внимательно подходить к применению антибиотиков, следить за их правильным использованием и сочетать их с пребиотиками и пробиотиками для восстановления здоровой микробной среды в организме. Таким образом, рациональное использование антибиотиков не только поможет в борьбе с инфекциями, но и сбережет микробную биоразнообразие, необходимое для поддержания общего здоровья и благополучия человека.
Видео по теме:
Вопрос-ответ:
Почему древние цивилизации использовали испорченные продукты для лечения?
Древние цивилизации использовали испорченные продукты для лечения, так как в процессе гниения или плесневения некоторые микроорганизмы производили вещества, которые могли иметь лечебный эффект на человеческий организм.
Какие именно продукты использовались для лечения в древние времена?
Для лечения в древние времена использовались различные продукты, такие как травы, мёд, молоко, мясо. Нередко наиболее эффективными оказывались испорченные продукты, такие как плесневелый хлеб, скисшее молоко, стухшее мясо.
Как древние цивилизации узнавали о свойствах испорченных продуктов?
Древние цивилизации могли случайно обнаружить свойства испорченных продуктов, когда люди испытывали их на себе в поисках лечения от различных болезней. Таким образом, с течением времени были выявлены положительные эффекты от употребления плесневелого хлеба, скисшего молока и других испорченных продуктов.
Почему испорченные продукты были эффективнее для лечения, чем свежие?
Испорченные продукты были эффективнее для лечения, так как в процессе гниения или плесневения в них могли образовываться бактерии или грибы, которые вырабатывали лечебные вещества, способствующие борьбе с различными инфекциями и болезнями.
Какие принципы использования антибиотиков можно выделить в древних цивилизациях?
В древних цивилизациях применение антибиотиков было основано на наблюдениях и опыте. Люди использовали травы, мед, животные продукты, а также испорченные продукты для лечения различных заболеваний. Они выбирали те продукты, которые оказывали наиболее эффективное лечебное действие, даже не имея научного объяснения для этого.